Цвет пламени[править | править код]
различный вид горелки Бунзена зависит от притока кислорода:1. богатая топливная смесь без предварительного смешивания с кислородом (подача кислорода закрыта) горит жёлтым коптящим рассеянным пламенем2. подача воздуха снизу почти перекрыта3. открыта в средней мере: смесь близка к стехиометрической4. подача воздуха максимальная: бедная смесь
Цвет пламени определяется излучением электронных переходов (например, тепловым излучением) различных возбужденных (как заряженных, так и незаряженных) частиц, образующихся в результате химической реакции между молекулами горючего и кислородом воздуха, а также в результате термической диссоциации. В частности, при горении углеродного горючего в воздухе, синяя часть цвета пламени обусловлена излучением частиц CN±n, красно-оранжевая — излучением частиц С2±n и микрочастиц сажи. Излучение прочих образующихся в процессе горения частиц (CHx±n, H2O±n, HO±n, CO2±n, CO±n) и основных газов (N2, O2, Ar) лежит в невидимой для человеческого глаза УФ и ИК части спектра. Кроме того, на окраску пламени сильно влияет присутствие в самом топливе, деталях конструкции горелок, сопел и так далее соединений различных металлов, в первую очередь натрия. В видимой части спектра излучение натрия крайне интенсивно и ответственно за оранжево-желтый цвет пламени, при этом излучение чуть менее распространенного калия оказывается на его фоне практически не различимым (поскольку большинство организмов имеют в составе клеток K+/Na+ каналы, то в углеродном горючем растительного или животного происхождения на 3 атома натрия приходится в среднем 2 атома калия).
Роль кислорода в образовании пламени
Кислород играет важнейшую роль в образовании и поддержании пламени. Без наличия кислорода горение невозможно. Он является необходимым реагентом для окисления топлива, что приводит к выделению энергии в виде тепла и света.
Кроме того, кислород играет роль окислителя в реакциях горения. Он вступает в химическую реакцию с топливом, перенося электроны и образуя окисленные продукты. Это позволяет поддерживать продолжение горения и обеспечивает обратный перенос энергии.
Кислород также влияет на структуру пламени. Он образует центральную зону пламени, называемую синей зоной или конусом горения. В этой области топливо полностью сгорает, именно здесь выделяется наибольшее количество тепла и света. Окружающая синяя зона представляет собой менее горячую зону с неполным сгоранием топлива и содержанием карбоновых соединений.
Соотношение кислорода и топлива влияет на цвет и яркость пламени. Недостаток кислорода может привести к образованию темной зоны пламени, где происходит неполное сгорание топлива и выделяются трудноосвобождающиеся продукты горения, такие как дым и сажа.
Важно отметить, что кислород может быть источником опасности, особенно в закрытых и плохо проветриваемых помещениях. При недостатке кислорода возможно возникновение асфиксии и угарного газа
Поэтому необходимо соблюдать правила безопасности при использовании огня и следить за нормальным содержанием кислорода в воздухе.
Огненный художник
При слове «костёр» вспыхивают не менее ярко ностальгические воспоминания: дым костра, создающий доверительную обстановку; красные и желтые огни, летящие к ультрамариновому небу; переливы язычков с голубого до рубиново-красного цвета; багровые остывающие угли, в которых печётся «пионерская» картошка.
Изменяющийся колер пылающего дерева сообщает о колебаниях температуры огня в костре. Тление дерева (потемнение) начинается со 150°. Возгорание (задымление) происходит в интервале 250-300°. При одинаковом поступлении кислорода породы при несовпадающих температурах. Соответственно, градус костра тоже будет отличаться. Берёза горит при 800 градусах, ольха — при 522°, а ясень и бук — при 1040°.

Но цвет огня также определяется химическим составом горящего вещества. Желтый и оранжевый вносят соли натрия. Химический состав целлюлозы содержит и соли натрия, и соли калия, придающие пылающим углям дерева красный оттенок. Романтические в древесном костре возникают из-за недостатка кислорода, когда вместо СО 2 образуется СО — угарный газ.
Энтузиасты научных опытов измеряют температуру огня в костре прибором под названием пирометр. Изготовляют три типа пирометров: оптические, радиационные, спектральные. Это бесконтактные приборы, разрешающие оценивать мощность теплового излучения.
Химические реакции в образующемся пламени
Пламя, как и большинство огней, является результатом химической реакции. Пламенная реакция происходит между топливом и окислителем, обычно кислородом из воздуха. При этом выделяется тепло и свет, что позволяет наблюдать пламя.
Когда топливо и окислитель смешиваются в определенных условиях, начинается окислительный процесс. Пламя включает в себя несколько стадий, каждая из которых связана с основными химическими реакциями:
- Инициация (зажигание): Начальная реакция, при которой возникает искра или иная инициирующая источник, которая разлагает молекулы топлива и окислителя на ионы и радикалы.
- Разделение на радикалы: Полученные ионы и радикалы реагируют друг с другом, образуя новые молекулы и радикалы. В результате образуются свободные радикалы, которые участвуют в следующей стадии пламени.
- Пульсирующая реакция: На этой стадии молекулы топлива и окислителя продолжают реагировать между собой и с радикалами, образуя более сложные молекулы и выделяя больше тепла и света.
- Обмен реакциями: На этой стадии тепло и свет от пламени поддерживают реакцию, и топливо и окислитель продолжают реагировать между собой. Это является самой энергетически активной стадией пламени.
Именно эти химические реакции вызывают основные характеристики пламени, такие как температура, цвет и яркость. Точное соотношение топлива и окислителя влияет на химическую реакцию, а, следовательно, и на характеристики пламени. Например, слишком много топлива может привести к копоти, тогда как недостаток топлива может затушить пламя.
Химические реакции, происходящие в пламени, также могут приводить к образованию новых соединений, таких как окиси азота и окиси углерода. Эти соединения на выходе пламени могут быть вредными и могут влиять на качество воздуха в окружающей среде.
Химические реакции в образующемся пламени
Топливо
Окислитель
Результат
Углеводороды
Кислород
СО2, H2O, тепло и свет
Металлы
Кислород
Окислы металлов, тепло и свет
Алкоголи
Кислород
СО2, H2O, тепло и свет
Это лишь некоторые примеры химических реакций, происходящих в образующемся пламени. Понимание этих реакций помогает контролировать и оптимизировать использование огня в различных приложениях, таких как кухонные плиты, автомобильные двигатели и промышленные печи.
Пламя в условиях невесомости[править | править код]
В условиях, когда ускорение свободного падения компенсируется центробежной силой, например, при полёте по орбите земли, горение вещества выглядит несколько иначе. Поскольку ускорение свободного падения компенсировано, сила Архимеда практически отсутствует. Таким образом, в условиях невесомости горение веществ происходит у самой поверхности вещества (пламя не вытягивается), а сгорание более полное. Продукты горения постепенно равномерно распространяются в среде. Это весьма опасно для систем вентилирования. Также серьёзную опасность представляют пудры, поэтому в космосе порошкообразные материалы не применяются нигде, кроме специальных опытов именно с порошками.
В струе воздуха пламя вытягивается и принимает привычный облик. Пламя газовых горелок благодаря давлению газа в условиях невесомости внешне также не отличается от горения в земных условиях.
Пламя в невесомости
Зоны пламени
Рассматривая, какое строение имеет пламя, выделяют три зоны: во-первых, предварительную, где начинается нагрев смеси, выходящей из отверстия горелки. После нее идет зона, где совершается процесс горения. Эта область захватывает верх конуса. Когда не хватает притока воздуха, сгорание газа идет частично. При этом образовываются оксид углерода и остатки водорода. Их горение происходит в третьей зоне, где присутствует хороший доступ кислорода.
Для примера представим строение пламени свечи.

Схема горения включает:
- первую — темную зону;
- вторую — зону свечения;
- третью — прозрачную зону.
Нитка свечи не поддается горению, а только совершается обугливание фитиля.
Строение пламени свечи представляет собой раскаленный поток газа, поднимающийся вверх. Процесс начинается с нагревания, пока не происходит испарение парафина. Зону, прилежащую к нити, именуют первой областью. Она имеет незначительное свечение голубого оттенка из-за избытка количества горючего материала, но малого поступления кислорода. Тут происходит процесс частичного сгорания веществ с образованием чадного газа, который затем окисляется.
Первую зону охватывает светящаяся оболочка. В ней находится достаточный объем кислорода, который способствует окислительной реакции. Именно здесь при интенсивном накаливании частичек оставшегося топлива и угольных частичек наблюдается эффект свечения.
Вторая зона охвачена чуть заметной оболочкой с высокой температурой. В нее проникает много кислорода, что содействует полному сгоранию топливных частичек.
Что такое пламя и почему огонь бывает разного цвета
Языки пламени представлены в виде раскаленных газов, иногда содержащих плазму и твердые элементы, в которых совершаются физико-химические перевоплощения реагентных элементов, вызывающие свечение, выделение тепла, самостоятельный нагрев.
Газообразная среда пламени состоит из заряженных ионов и радикалов, что объясняет возможность электропроводности пламени и его взаимодействие с электромагнитными полями. По такому принципу производятся приборы, обладающие способностью при помощи электромагнитного излучения приглушать пламя, оторвать его от горючих материалов и даже изменить форму.
Причины разноцветности пламени
Включив газовую конфорку и поджигая выходящий газ, мы видим голубоватый огонь? В процессе горения газ распадается на кислород и углерод, выделяя при этом угарный газ, который и является причиной голубого цвета.
подожженная простая пищевая соль – в огне выдает желтые и красные цвета? В состав соли входит хлорид натрия, при горении создающий желто-оранжевые языки пламени. Любой деревянный предмет или костер из дров будут гореть таким же цветом, так как в составе древесного материала находится большое количество подобных солей.
Есть у огня и зеленые оттенки, ? Их появление означает то, что в горящих предметах содержатся фосфор или медь. Причем медное пламя будет ярким и слепящим, близким к белому. Причиной зеленого пламени может стать наличие в предметах горения бария, молибдена, фосфора, сурьмы. Синий цвет зависит от селена или бора.
Огонь без признаков цвета можно увидеть только в лабораторных условиях. Понять, что что-то горит, возможно только по легкому колебанию воздуха и выделяемому теплу.
Помните! Огонь очень опасен. Распространяется молниеносно. Никогда не играйте с огнем. Находиться рядом с огнем можно только в присутствии взрослых!
Полезно знать
- Все газовые приборы представляют собой повышенную . По этой причине не помешает узнать некоторые признаки поломок, способы их устранения. Определять неисправности будем по цвету пламени.
- Если ваша горелка при работе издает желтое пламя или оранжевое – это признак того, что не хватает воздушной смеси. Чтобы горение газа проходило правильно, максимально выдавала тепло, необходимо достаточное количество воздуха, который перемешивается с газом в главной горелке.
- Нарушение баланса в смеси топлива и воздуха может произойти по разным причинам. Воздушные отверстия засорились пылью, не давая проходить воздушным потокам. Пылевые накопления, сгорая, создают желтоватый или оранжевый цвет пламени.
- Желтизна пламени возможна и в том случае, газовое оборудование приобретено неправильно. При сгорании любого топлива выделяется угарный газ. Колонки, выдающие при работе синее пламя, выдают низкий уровень СО. Наличие оранжевого или красного огня говорят об обратном.
- При отравлении угарными газами наблюдаются симптомы, как при гриппе – головные боли, тошнота, головокружения. Угарный газ опасен тем, что его присутствие зачастую остается незамеченным людьми, так как он не отличается наличием цвета или запаха.
Теперь вы знаете, почему огонь бывает разного цвета, от чего зависит цвет пламени
Обратите внимание: если мы наблюдаем на газовом приборе желтое, красное или оранжевое пламя – это можно считать сигналом опасности. Обнаружив это, необходимо вызвать квалифицированных специалистов, которые определят причину и устранят неисправность газового оборудования
Температура огня заставляет в новом свете увидеть привычные вещи — вспыхнувшую белым спичку, голубое свечение горелки газовой печки на кухне, оранжево-красные язычки над пылающим деревом. Человек не обращает внимания на огонь, пока не обожжёт кончики пальцев. Или не спалит картошку на сковороде. Или не прожжёт подошву кроссовок, сохнущих над костром.
Когда первая боль, испуг и разочарование проходят, наступает время философских размышлений. О природе, цветовой гамме, температуре огня.
Горение спиртовки
Для химических экспериментов часто используют небольшие резервуары со спиртом. Их называют спиртовками. Фитиль горелки пропитывается залитым через отверстие жидким топливом. Этому способствует давление капиллярное. При достижении свободной верхушки фитиля, спирт начинает испаряться. В парообразном состоянии он поджигается и горит при температуре не более 900 °C.
Пламя спиртовки имеет обычную форму, оно практически бесцветное, с небольшим оттенком голубого. Его зоны не так четко видны, как у свечки.
У спиртовой горелки, названной в честь ученого Бартеля, начало огня располагается над калильной сеткой горелки. Такое заглубление пламени приводит к уменьшению внутреннего темного конуса, а из отверстия выходит средний участок, который считается самым горячим.

Строение — пламя
Строение пламени при горении углеводородов в кислороде или в воздухе характеризуется наличием трех зон: ядра, средней зоны, факела.
|
Жаропроизводительность ( в воздухе различных горючих газов. |
Строение пламени зависит от типа газового устройства и способа сжигания газа. Различают сжигание газа светящимся пламенем, несветящимся пламенем и беспламенное сжигание.
Строение пламени может быть различно и зависит от метода сжигания газа и типа газового устройства.
|
Сушильный шкаф с электрообогревом и терморегулятором. |
Зная строение пламени, легко сделать практический вывод. Пользуясь горелкой, не следует нагрева емыи предмет глубоко опускать в пламя; необходимо его помещать так, чтобы верхняя, наиболее горячая часть пламени лишь слегка касалась предмета.
|
Строение и состав ацетилено-кислородного пламени. |
На рис. 219 показано строение пламени.
Затем на схеме преподаватель показывает строение несве-тящегоея пламени, зону подготовки пламени при полном горении газовоздушной смеси в результате предварительного частичного смешения газа с воздухом-образующего короткий факел голубовато-фиолетового цвета с зеленовато-голубым ядром в форме конуса; В конусе нагревается выходящая из горелки газовоздушная см. есь, которая на поверхности конуса сгорает. Вследствие недостатка воздуха происходит неполное, сгорание газа с образованием окиси углерода и части несгоревшего водорода, которые догорают в зоне догорания при помощи кислорода вторичного воздуха, окружающего факел.
Общие закономерности горения, а также строение пламени — при использовании в качестве горючих других углеводородов, являются подобными. Сжигание горючих смесей этих газов с кислородом характеризуется наличием светящегося ядра и средней зоны, в большей или меньшей степени отделяющейся по виду от факела.
|
Сопоставление различных горючих газов. |
На рис. Ill А, а изображено строение пламени предварительно перемешанной внутри горелки смеси ацетилена и кислорода, получающееся при обычной конструкции газосварочной горелки с одним общим отверстием для вытекания. Такое пламя ( так же, как и пламя при горении других углеводородов в кислороде или воздухе) имеет три зоны.
По соотношению газов в смеси сварочное пламя делят на нормальное, науглероживающее и окислительное. Схема строения ацетплено-кислородного пламени с различным соотношением р приведена на фиг.
Метод основан на характерных реакциях, протекающих под действием высокотемпературного пламени. В строении пламени различают три конуса: 1) внутренний низкотемпературный, содержит вещество, напр, свечи, в парообразном состоянии; 2) средний, сравнительно высокотемпературный ( восстановительный) содержит большое количество неполностью окисленных продуктов горения, напр. СО, а также С, Н и Н20; 3) наружный высокотемпературный ( окислительный) состоит из продуктов полного сгорания и избытка кислорода. При помощи паяльной трубки воздух, вдуваемый в пламя, усиливает горение и реакционная способность восстановительного и окислительного конусов значительно повышается. Известны также характерные реакции на отдельные элементы, не включенные в перечисленные выше группы.
Под устойчивостью пламени понимается способность его сохранять при небольших изменениях скорости горящей струи свое нормальное положение вблизи выходного отверстия. Характер и строение пламени, которое возникает при горении ламинарной струи данной смеси, нам уже известны: возле выходного отверстия трубки образуется голубой конус первичного горения, над ним возникает вторичное диффузионное пламя. Начнем увеличивать скорость выхода газовоздушной смеси, оставляя неизменным ее состав. При этом, как и следовало ожидать, конус первичного горения начнет удлиняться, так как точка, в которой осевая скорость газовоздушной струи равна по величине направленной навстречу скорости распространения пламени и в которой, следовательно, находится вершина этого конуса, сместится вверх, по направлению движения газовоздушной струи. При этом суммарная поверхность конуса увеличится, что как раз и соответствует увеличению количества газа, сгорающего на этой поверхности.
Процесс образования пламени
Пламя — это явление горения, при котором выделяются видимый свет, тепло и звук. Основными компонентами пламени являются горючее вещество, окислитель и источник зажигания.
1. Инициация горения. Процесс образования пламени начинается с инициации горения. Для этого необходимо наличие источника зажигания — открытого огня, искры или высокой температуры.
2. Выделение газов. При воздействии источника зажигания на горючее вещество происходит его нагревание. В результате молекулы горючего вещества начинают разделяться на более легкие компоненты — газы. Это происходит из-за нарушения химических связей в молекулах горючего вещества.
3. Распространение пламени. Выделенные газы поднимаются вверх от источника зажигания, образуя горючий газовый слой. В этом слое смесь газов и окислителя находится в горячем пламени. Горячие газы нагревают окружающую среду и поднимаются вверх, создавая конвекционный поток, который поддерживает распространение пламени вверх.
4. Окисление и реакции горения. В процессе распространения пламени происходят окислительные реакции между горючими газами и окислителем. При этом выделяется тепло и является источником энергии пламени. Также при горении образуются продукты сгорания, такие как углекислый газ, вода, дым и твердые остатки.
5. Видимый свет пламени. Видимый свет пламени образуется благодаря нагреванию газов до высоких температур. При этом некоторые электроны в молекулах газов переходят на более высокие энергетические уровни и затем возвращаются в исходное состояние, испуская энергию в виде света. Различные химические элементы в горящем газовом слое определяют цвет пламени.
Таким образом, процесс образования пламени представляет собой сложную цепную реакцию окисления горючего вещества с участием окислителя и источника зажигания.
Характеристика
В основе классификации пламени лежат следующие характеристики:
- состояние агрегатное сгорающих соединений. Они бывают газообразной, аэродисперсной, твердой и жидкой формы;
- тип излучения, которое может быть бесцветным, светящимся и окрашенным;
- распределительная скорость. Существует быстрое и медленное распространение;
- высота пламени. Строение может быть коротким и длинным;
- характер передвижения реагирующих смесей. Выделяют пульсирующее, ламинарное, турбулентное перемещение;
- визуальное восприятие. Вещества горят с выделением коптящего, цветного или прозрачного пламени;
- температурный показатель. Пламя может быть низкотемпературным, холодным и высокотемпературным.
- состояние фазы топливо – окисляющий реагент.
Возгорание происходит в результате диффузии или при предварительном перемешивании активных компонентов.

Пламя: строение и структура
Для определения внешнего вида описываемого явления достаточно зажечь газовую горелку. Появившееся несветящееся пламя нельзя назвать однородным. Визуально можно выделить три его основные области. Кстати, изучение строения пламени показывает, что различные вещества горят с образованием различного типа факела.
При горении смеси из газа и воздуха вначале происходит формирование короткого факела, цвет которого имеет голубые и фиолетовые оттенки. В нем просматривается ядро — зелено-голубое, напоминающее конус. Рассмотрим это пламя. Строение его разделяется на три зоны:
- Выделяют подготовительную область, в которой происходит нагревание смеси из газа и воздуха при выходе из отверстия горелки.
- За ней следует зона, в которой происходит горение. Она занимает верхушку конуса.
- Когда имеется недостаток воздушного потока, газ сгорает не полностью. Выделяется углерода двухвалентный оксид и водородные остатки. Их догорание протекает в третьей области, где есть кислородный доступ.
Теперь отдельно рассмотрим разные процессы горения.
Температура пламени[править | править код]
- Температура воспламенения для большинства твёрдых материалов — 300 °С.
- Температура пламени в горящей сигарете — 250–300 °С.[источник не указан 960 дней]
- Температура пламени спички 750–1400 °С; при этом 300 °С — температура воспламенения дерева, а температура горения дерева равняется примерно 500–800 °С.
- Температура горения пропан-бутана — 800–1970 °С.
- Температура пламени керосина — 800 °С, в среде чистого кислорода — 2000 °С.
- Температура горения бензина — 1300–1400 °С.
- Температура пламени спирта не превышает 900 °С.
- Температура горения магния — 2200 °С; значительная часть излучения в УФ-диапазоне.
Наиболее высокие известные температуры горения: дицианоацетилен C4N2 5’260 К (4’990 °C) в кислороде и до 6’000 К (5’730 °C) в озоне; дициан (CN)2 4’525 °C в кислороде.
Так как вода обладает очень большой теплоёмкостью, отсутствие водорода в горючем исключает потери тепла на образование воды и позволяет развить бо́льшую температуру.
Цветовая характеристика
Излучения различных цветов пламени, вызывается электронными переходами. Их еще называют тепловыми. Так, в результате горения углеводородного компонента в воздушной среде, синее пламя обусловлено выделением соединения H-C. А при излучении частичек C-C, факел окрашивается в оранжево-красный цвет.
Трудно рассмотреть строение пламени, химия которого включает соединения воды, углекислого и угарного газа, связь OH. Его языки практически бесцветны, так как вышеуказанные частички при горении выделяют излучения ультрафиолетового и инфракрасного спектра.
Окраска пламени взаимосвязана с температурными показателями, с наличием в нем ионных частиц, которые относятся к определенному эмиссионному или оптическому спектру. Так, горение некоторых элементов приводит к изменению цвета огня в горелке. Отличия в окрашивании факела связаны с расположением элементов в разных группах системы периодической.
Огонь на наличие излучений, относящихся к видимому спектру, изучают спектроскопом. При этом было установлено, что простые вещества из общей подгруппы оказывают и подобное окрашивание пламени. Для наглядности используют горение натрия в качестве теста на данный металл. При внесении его в пламя, языки становятся ярко-желтыми. На основании цветовых характеристик выделяют натриевую линию в эмиссионном спектре.
Для щелочных металлов характерно свойство быстрого возбуждения светового излучения атомарных частиц. При внесении труднолетучих соединений таких элементов в огонь горелки Бунзена происходит его окрашивание.
Спектроскопическое исследование показывает характерные линии в области, видимой для глаза человека. Быстрота возбуждения светового излучения и простое спектральное строение тесно взаимосвязаны с высокой электроположительной характеристикой данных металлов.
Изучаем огонь на собственной кухне
Кухонные газовые плиты работают на двух видах топлива:
- Магистральный природный газ метан.
- Пропан-бутановая сжиженная смесь из баллонов и газгольдеров.
Химический состав топлива определяет температуру огня газовой плиты. Метан, сгорая, образует огонь мощностью 900 градусов в верхней точке.
Сжигание сжиженной смеси даёт жар до 1950°.
Внимательный наблюдатель отметит неравномерность раскраски язычков горелки газовой плиты. Внутри огненного факела происходит деление на три зоны:
- Тёмный участок, расположенный возле конфорки: здесь нет горения из-за недостатка кислорода, а температура зоны равна 350°.
- Яркий участок, лежащий в центре факела: горящий газ разогревается до 700°, но топливо сгорает не до конца из-за недостатка окислителя.
- Полупрозрачный верхний участок: достигает температуры 900°, и сгорание газа полноценное.
Цифры температурных зон огневого факела приведены для метана.
Температурные показатели
Каждая зона огня свечи или горелки имеет свои значения, обусловленные поступлением кислородным молекул. Температура открытого пламени в разных его частях колеблется от 300 °C до 1600 °C.
Примером служит пламя диффузионное и ламинарное, которое образовано тремя оболочками. Конус его состоит из темного участка с температурой до 360 °C и недостатком окисляющего вещества. Над ним располагается зона свечения. Ее температурный показатель колеблется от 550 до 850 °C, что способствует разложению термическому горючей смеси и ее горению.
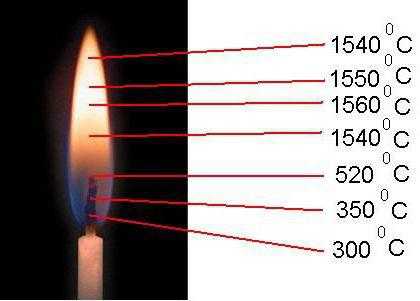
Внешняя область едва заметная. В ней температура пламени доходит до 1560 °C, что обусловлено природными характеристиками топливных молекул и быстротой поступления окисляющего вещества. Здесь горение наиболее энергичное.
Вещества воспламеняются при разных температурных условиях. Так, металлический магний горит только при 2210 °С. Для многих твердых веществ температура пламени около 350 °С. Возгорание спичек и керосина возможно при 800 °С, тогда как древесины — от 850 °С до 950 °С.
Сигарета горит пламенем, температура которого варьируется от 690 до 790 °С, а в пропан-бутановой смеси — от 790 °С до 1960 °С. Бензин воспламеняется при 1350 °С. Пламя горения спирта имеет температуру не более 900 °С.
Всегда кажется, что огонь имеет два оттенка – красный и желтый. Но если присмотреться внимательно, то можно приметить, что цветность огня различается от того, какой предмет горит. Входящие в его состав вещества и выдают свои цвета пламени. Итак, почему огонь бывает разного цвета, от чего зависит цвет пламени?
Сварочное пламя
Данный вид огня образуется в результате сгорания смеси из газа или пара жидкости с кислородом чистого воздуха.

Примером служит формирование пламени кислородно-ацетиленового. В нем выделяют:
- зону ядра;
- среднюю область восстановления;
- факельную крайнюю зону.
Так горят многие газокислородные смеси. Различия в соотношении ацетилена и окислителя приводят к разному типу пламени. Оно может быть нормального, науглероживающего (ацетиленистого) и окислительного строения.
Теоретически процесс неполного сгорания ацетилена в чистом кислороде можно охарактеризовать следующим уравнением: HCCH + O 2 → H 2 + CO +CO (для реакции необходима одна моль O 2) .
Полученный же молекулярный водород и угарный газ реагируют с воздушным кислородом. Конечными продуктами является вода и оксид четырехвалентного углерода. Уравнение выглядит так: CO + CO + H 2 + 1½O 2 → CO 2 + CO 2 +H 2 O. Для этой реакции необходимо 1,5 моля кислорода. При суммировании O 2 получается, что 2,5 моль затрачивается на 1 моль HCCH. А так как на практике трудно найти идеально чистый кислород (часто он имеет небольшое загрязнение примесями), то соотношение O 2 к HCCH будет 1,10 к 1,20.
Когда значение пропорции кислорода к ацетилену меньше 1,10, возникает науглероживающее пламя. Строение его имеет увеличенное ядро, очертания его становятся расплывчатыми. Из такого огня выделяется копоть, вследствие недостатка кислородных молекул.
Если же соотношение газов больше 1,20, то получается окислительное пламя с кислородным избытком. Лишние его молекулы разрушают атомы железа и другие компоненты стальной горелки. В таком пламени ядерная часть становится короткой и имеет заострения.
Кислород
Кислород – химический элемент с атомным номером 8 и символом O. Он является частью воздуха и входит в состав многих органических и неорганических соединений.
Кислород является ключевым компонентом в процессе горения. Он поддерживает жизнедеятельность организмов, улучшает окислительные процессы и выполняет ряд других важных функций. В атмосфере Земли кислород находится в виде двухатомных молекул (O2), которые обеспечивают дыхание живых существ.
Основные свойства кислорода:
- Кислород обладает высокой электроотрицательностью, что позволяет ему образовывать связи с другими электроотрицательными элементами, такими как водород.
- Он является хорошим окислителем и может быть вовлечен в множество химических реакций.
- В больших количествах кислород ядовит для многих микроорганизмов и бактерий.
- Кислород имеет низкую плотность и является газообразным при нормальных условиях.
Процессы, связанные с кислородом:
- Дыхание: Кислород необходим для процесса дыхания организмов, включая людей и животных. При вдыхании воздуха, кислород попадает в легкие, где он переходит в кровь и распределяется по организму.
- Горение: Кислород играет ключевую роль в процессе горения. Он поддерживает сгорание топлива, такого как древесина, уголь или бензин. Без кислорода огонь не может существовать.
- Фотосинтез: Растения используют кислород в процессе фотосинтеза для превращения углекислого газа и солнечной энергии в глюкозу и кислород. Это процесс позволяет растениям производить пищу и выделять кислород в атмосферу.
Значение кислорода для жизни:
| Жизненные процессы | Зависимость от кислорода |
|---|---|
| Дыхание | Необходим для поддержания жизни и обмена веществ |
| Разгар горения | Без кислорода огонь не может существовать |
| Фотосинтез | Растения используют кислород и выделяют его в атмосферу |
От чего зависит строение пламени?
Оно мерцает разными цветами, в то время, когда фитиль сгорает, проходя сквозь тающий воск. Огонь требует доступ кислорода. Когда свеча горит, в середину пламени, возле дна, много кислорода не попадает. Поэтому оно выглядит более темным. Но вершина и бока получают много воздуха, поэтому там пламя очень яркое. Оно нагревается более чем 1370 градусов по Цельсию, это делает пламя свечи в основном желтого цвета.
А в камине или в костре на пикнике можно увидеть даже больше цветов. Дровяной огонь горит при температуре ниже, чем свеча. Поэтому он выглядит больше оранжевым, чем желтым. Некоторые частицы углерода в огне очень горячие и придают ему желтизны. Минералы и металлы, такие как кальций, натрий, медь, нагреты до высоких температур, придают огню разнообразные цвета.
















